Κάποτε πιστεύαμε πως το γήρας είναι μια μοναχική, αδιάκοπη διαδικασία. Υποθέταμε, ότι κάθε κύτταρο αποσύρεται σιωπηλά, αφήνοντας τα άλλα κύτταρα, να κάνουν την δουλειά τους. Αυτά τα κύτταρα μπαίνουν σε μία κυτταρική αδράνεια. Είναι ζωντανά μεν, αλλά υπολειτουργούν, καταλαμβάνοντας ζωτικό χώρο (όπως κάποιοι δημόσιοι υπάλληλοι) οδηγώντας σε μία οργανική υπολειτουργία. Με το πέρας του χρόνου ο αριθμός των αδρανών κυττάρων αυξάνεται εις βάρος των ενεργών και επιταχύνεται παρουσία χρόνιων φλεγμονών, επιγενετικών αλλαγών κλπ.
Μία μικρή πρωτεΐνη ονόματι ReHMGB1, που κάποτε θεωρούνταν απλώς ένα σήμα ενεργοποίησης της φλεγμονής ή συγκεκριμένης γονιδιακής έκφρασης, ανάλογα που βρισκόταν – στον πυρήνα ή στο κυτταρόπλασμα – αποκαλύφθηκε ως ένας τροβαδούρος του κυτταρικού γήρατος. Όταν τα κύτταρα γεράσουν και γίνουν ιδιότροπα, δεν κάθονται απλώς άπραγα. Απελευθερώνουν ReHMGB1 στο αίμα, όπου ταξιδεύει σαν αγγελιαφόρος της παρακμής, ψιθυρίζοντας σε μακρινά όργανα: «Ήρθε η ώρα, φίλοι μου. Ώρα να επιβραδύνετε».
Το γήρας όμως, μοιάζει περισσότερο με μία προπαγανδιστική ραδιοφωνική εκπομπή με παρουσιαστή την ReHMGB1. Είναι γεγονός (!) Σε μία μελέτη που δημοσιεύτηκε το 2023, αποδείχτηκε ότι τα ανθρώπινα όργανα δε γερνάνε την ίδια περίοδο και με την ίδια ταχύτητα. Μάλιστα, οι αρτηρίες είναι το πρώτο σύστημα που γερνάει, ξεκινώντας στα 50 έτη, με κύριο ύποπτο την πρωτεΐνη GAS6 που κυκλοφορεί επίσης στο αίμα. Αυξημένη GAS6 έχει φανεί να εμπλέκεται σε περιστατικά θρόμβωσης, αυτοάνοσων νοσημάτων και χρόνιας φλεγμονής.
It’s in the blood (!) Άρρητα συνδεδεμένο με το παρθενικό μου άρθρο, Βρυκόλακες 2.0 (!!) Χαίρομαι για αυτό, μπορεί και εσείς. Σε μία πρόσφατη εργαστηριακή μελέτη, ερευνητές στην Νότιο Κορέα (K-pop forever) παρατήρησαν ότι η αυξομείωση της συγκεκριμένης πρωτεΐνης στο αίμα ποντικών είναι άρρητα συνδεδεμένη με την κυτταρική γήρανση, προερχόμενη από την κυτταρική αδράνεια, κάτι που η μη-οξειδωμένη μορφή (Re) της HMGB1 φαίνεται να έχει ψηλά στην ατζέντα της (Εικόνα 1).
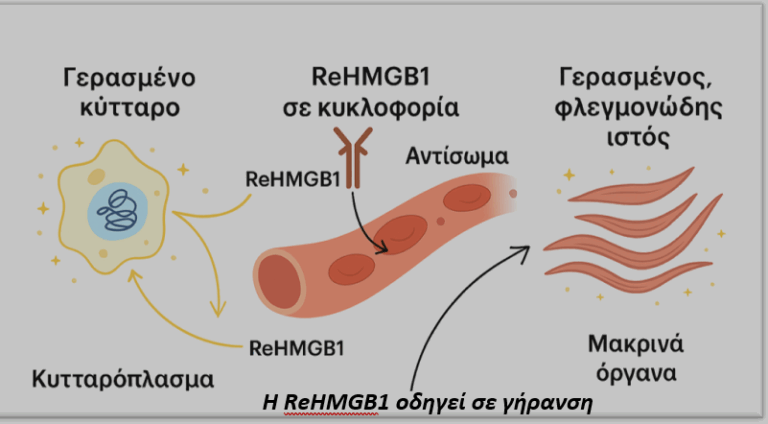
Χορήγησαν λοιπόν, σε ανυποψίαστα νεαρά ποντίκια μία δόση ReHMGB1 στο κυκλοφορικό τους σύστημα, και μία εβδομάδα αργότερα παρατήρησαν αυξημένη κυτταρική αδράνεια (ο προάγγελος της κυτταρικής γήρανσης) σε καρδιά, συκώτι, μύες, στομάχι κλπ. Ειδική μνεία δόθηκε στην εμπόδιση των σκελετικών μυών να αναγεννηθούν μετά από τραυματισμό, στα παραπάνω πειράματα, ακόμη και στα νεαρά ποντίκια.
Δεν είναι ποιητικό; Η ReHMGB1 δεν σκοτώνει κύτταρα. Τα πείθει, σιγά-σιγά, απλά να σταματήσουν να προσπαθούν. Είναι σαν το Lullaby των Cure — αργό, μελαγχολικό, πειστικό. Ένα βιντεοκλίπ που όταν το παρακολουθούσαμε στο MTV, μέναμε με το στόμα ανοικτό.
Αλλά να η ανατροπή: οι ίδιοι επιστήμονες ανακάλυψαν πως αν μπλοκάρεις τη ReHMGB1, μπορείς να διακόψεις αυτή την εκστρατεία συστημικής παραίτησης. Αυτό μπορεί να επιτευχθεί είτε με αντισώματα ή με τροποποίηση της οξειδοαναγωγικής της κατάστασης, οι ιστοί που ήταν έτοιμοι να τα παρατήσουν… δεν το κάνουν. Οι μύες αναγεννούνται. Η φλεγμονή υποχωρεί. Το σώμα θυμάται πώς να επουλώνεται. Πράγματι, στα πειράματα όπου ένα συγκεκριμένο αντίσωμα ‘’μπλόκαρε’’ την ReHMGB1, σε ηλικιωμένα τώρα ποντίκια, έδειξαν ότι η λειτουργικότητα του σκελετικού μυός μετά από τραυματισμό τού, μειώθηκε κατά 50%-80% περισσότερο απ’ ότι στα ηλικιωμένα ποντίκια που δεν τους είχε χορηγηθεί το αντίσωμα αλλά είχαν τραυματιστεί. Σε κάποιες παρατηρήσεις, μάλιστα, φάνηκε να υπάρχει και βελτίωση της κινητικότητας σε σχέση με τα ατραυμάτιστα ποντίκια ίδιας ηλικίας (π.χ. τρέξιμο).
Τι σημαίνει αυτό για εμάς — σημαίνει πως το γήρας δεν είναι απλώς βιολογική μοίρα. Είναι αφήγηση — και όπως κάθε καλή ιστορία, μπορεί να υποστεί επεξεργασία. Πρόσφατες μελέτες έδειξαν ότι στους ανθρώπους άνω των 70 ετών, η HMGB1 είναι σημαντικά αυξημένη, στο αίμα. Επιπλέον, υπάρχει μία συγκεκριμένη περιοχή στο μέρος της HMGB1 όπου εφάπτεται στο DNA (ονομάζεται Box A) όπου φαίνεται να ‘’ξυπνά’’ τα ληθαργικά ανθρώπινα βλαστοκύτταρα. Όμως, δεν γνωρίζουμε ακόμη τις επιπτώσεις που θα έχει η απουσία της στο ανοσοποιητικό σύστημα και στην επούλωση τραυμάτων. Φυσικά, μπορεί να λειτουργήσει σαν βιοδείκτης γήρανσης και εφόσον είναι γνωστός ο μηχανισμός λειτουργίας της, είναι θέμα χρόνου και οι στοχευμένες κλινικές μελέτες σε υγιείς ηλικιωμένους με σαρκοπενία, για παράδειγμα.
Το πιθανό αποτέλεσμα; Εικάζω ότι θα βοηθήσει σε μία σημαντική επιβράδυνση του γήρατος σε συνδυασμό με άλλα φάρμακα. Το μπλοκάρισμα της ReHMGB1 δεν σε κάνει αθάνατο. Δεν σβήνει τις ρυτίδες ή τις τύψεις. Aλλάζει όμως τον ρυθμό. Μετατρέπει το μοιρολόι σε μία μελωδική μπαλάντα των 80’s (Whitesnake). Δίνει μερικούς στίχους παραπάνω πριν το τελικό ρεφρέν. Και ίσως αυτό να είναι αρκετό.
Το πόσο δυνατά θα τραγουδήσει ο βάρδος του γήρατος, θα φανεί στα προσεχή έτη, όπου θα δοκιμαστεί η εν λόγω πειραματική θεραπεία σε χιμπατζήδες για πιθανές παρενέργειες. Στα ποντίκια πάντως δεν είχε, τουλάχιστον βραχυπρόθεσμα. Βέβαια, όπως και όλες οι πρωτεΐνες πασπαρτού, θα πρέπει να μελετηθούν εις βάθος, διότι η εξάλειψη τους μπορεί να οδηγήσει στα ακριβώς αντίθετα αποτελέσματα. Οπότε, εις υγείαν της ReHMGB1 – της πρωτεΐνης που μας έδειξε πως το γήρας είναι τραγούδι. Και στην επιστήμη – που μας έδωσε το μικρόφωνο.
Επιλεγμένη βιβλιογραφία
Shin JW, Jang DH, Kim SY, et al. Propagation of senescent phenotypes by extracellular HMGB1 is dependent on its redox state. Metabolism. 2025;168:156259. doi: 10.1016/j.metabol.2025.156259
Ruggieri, E., Di Domenico, E., Locatelli, A. G., Isopo, F., Damanti, S., De Lorenzo, R., Milan, E., Musco, G., Rovere-Querini, P., Cenci, S., & Vénéreau, E. (2024). HMGB1, an evolving pleiotropic protein critical for cellular and tissue homeostasis: Role in aging and age-related diseases. Ageing Research Reviews, 102, 102550. https://doi.org/10.1016/j.arr.2024.102550
EI, Z. Z., MUTIRANGURA, A., ARUNMANEE, W., & CHANVORACHOTE, P. (2023). The Role of Box A of HMGB1 in Enhancing Stem Cell Properties of Human Mesenchymal Cells: A Novel Approach for the Pursuit of Anti-aging Therapy. In Vivo, 37(5), 2006. https://doi.org/10.21873/invivo.13298
Comprehensive human proteome profiles across a 50-year lifespan reveal aging trajectories and signatures. Ding, Yingjie et al. Cell, Volume 188, Issue 20, 5763 – 5784.e26. 10.1016/j.cell.2025.06.047







